Sales minerales
Las sales minerales y las vitaminas no proporcionan energía química pero son componentes necesarios en la dieta, porque participan como cofactores y coenzimas en muchas reacciones enzimáticas. Además, algunos minerales como el calcio son indispensables para la estructura ósea, el cual participa también como activador y señal metabólica para las células musculares y nerviosas. El sodio, el cloruro y el bicarbonato son componentes principales de los líquidos extracelulares. Estos contribuyen en la formación de un ambiente que permita la vida celular en las mejores condiciones, para el cual todas las células vivas se han adaptado a través de miles y millones de años. Estos son sólo algunos ejemplos de las múltiples funciones que desempeñan determinados elementos o compuestos en el organismo.
Agua
El agua, aunque no aporta energía química, es de los nutrimentos más importantes para el organismo. Es el componente fundamental de todos los compartimentos líquidos y representa el mayor porcentaje del peso corporal.
Nutricionalmente tiene grandes repercusiones en el organismo, por ejemplo ¿sabías que está demostrado que en ausencia de ingesta de agua, un organismo humano adulto moriría en un plazo de 5 a 10 días? ¡Imagínate! ¡Sólo resistiríamos hasta 10 días sin tomar agua!
Durante la digestión y la absorción, el agua en estado líquido, mantiene disueltos o en suspensión los demás componentes de los alimentos al interior del cuerpo. El agua, también sirve como fase móvil en el acarreo de todos los nutrimentos hasta las células, entra con ellos y participa en el metabolismo y en la estructura de las células (como el citoplasma); sale de las células llevando los productos de desecho, aún disueltos en agua, a los órganos de excreción, ¿recuerdas cuáles? ¡Claro! La orina y el sudor. ¿Quieres conocer más sobre la molécula del agua?
En el agua se realizan la mayoría de los procesos celulares en los organismos, puede afirmarse que la conformación que toman las moléculas dentro de las células depende del agua. Las características peculiares de ésta derivan de su estructura química particular, en la cual los dos hidrógenos y el oxígeno se encuentran formando un tetraedro irregular en el que el oxígeno ocupa el centro y los hidrógenos, junto con los dos orbitales del oxígeno no compartido, están dirigidos hacia los vértices restantes. La diferencia de electronegatividades entre el oxígeno y los hidrógenos hace que los enlaces entre ellos sean covalentes polares, dando cargas parciales positivas y negativas a la molécula, convirtiéndola así en un dipolo. Esta característica permite que exista una fuerza de atracción entre los extremos cargados opuestamente de las moléculas vecinas.
La atracción entre las moléculas de agua permite que se establezcan enlaces débiles llamados enlaces o puentes de hidrógeno, éstos configuran redes cuya existencia proporciona al agua sus propiedades fisicoquímicas características.
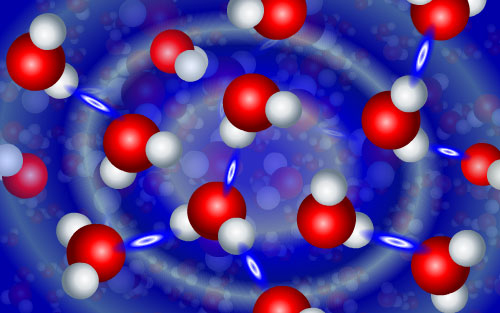
Fuente: Flickr https://www.flickr.com/photos/nsf_beta/7369047118
Todas esas propiedades permiten que el agua desempeñe muy variadas funciones en los seres vivos. Por ejemplo, servir como medio universal de solución, de suspensión y de reacción para todas las moléculas. O bien, intercambiar cantidades importantes de calor sin mucha variación de su temperatura, esto le permite mantener constante la temperatura del organismo y controlarla mediante los fenómenos de vasoconstricción y vasodilatación, como en la sudoración.
Recuerda cuándo haces ejercicio ¿Qué sucede después de un rato de hacer ejercicio? ¡Efectivamente! Comenzamos a sudar.
¿Qué sucedería si no sudamos cuando hacemos ejercicio? El ejercicio genera calor y provoca aumento de la temperatura corporal.
Con el sudor, el organismo pierde calor y regula la temperatura corporal. El transporte de sustancias entre los diversos órganos y tejidos del cuerpo humano se hace por el plasma y por los líquidos extracelulares, ambos de naturaleza acuosa.
Las interacciones del agua con las diversas moléculas permiten el mantenimiento de las estructuras celulares. La presencia de partículas en solución va a modificar las propiedades características del agua, lo que da origen a las propiedades coligativas de las soluciones; propiedades que dependen del número de partículas en la solución y no de su naturaleza. Entre éstas, la más notable es la aparición de la presión osmótica.