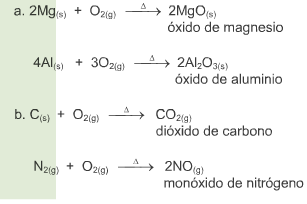
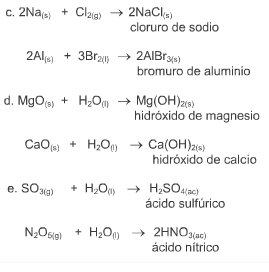
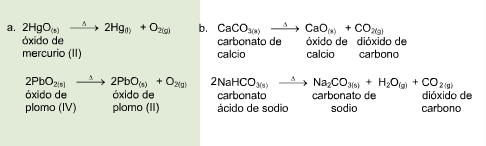
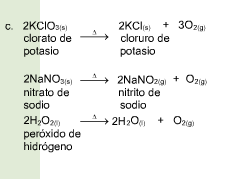
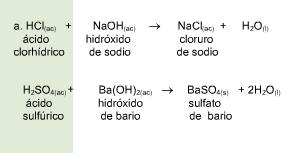
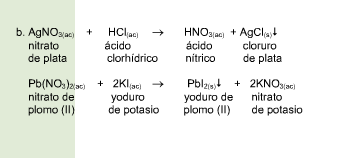
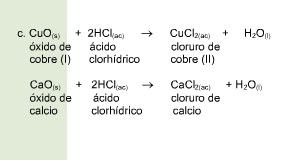
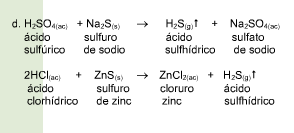
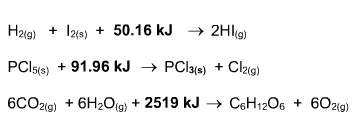
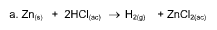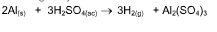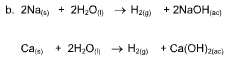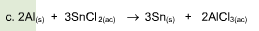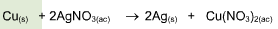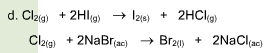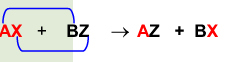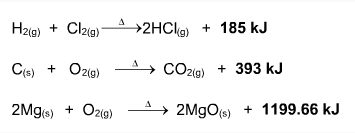Una reacción química toma lugar cuando los materiales que se usan al inicio (reactivos) se cambian a nuevos materiales (productos).
En la vida diaria ocurren muchas reacciones químicas, por ejemplo la fermentación, la combustión, la corrosión de metales (clavos oxidados), la efervescencia de pastillas, la oxidación de las frutas (oscurecimiento del plátano o de la manzana), entre muchas otras. Los símbolos más utilizados en una ecuación química son:
| Símbolo | Significado |
|---|---|
| ↑ | Se desprende |
| ↓ | Se precipita |
| → | Línea de reacción, significa se transforma en |
 | Calor |
Los tipos más comunes de reacciones químicas son: síntesis, descomposición, sustitución simple y sustitución doble .